Atom mengandung sebuah nukleus (inti) kecil yang
padat yang dikelilingi elektron-elektron. Inti ini bermuatan positif dan
merupakan sebagian besar dari massa atom tersebut. Inti terdiri atas jumlah
proton, yang bermuatan positif, dan neutron yang netral. (pengecualian
satu-satunya ialah hidrogen, yang intinya hanya memiliki satu proton). Dalam
atom netral, muatan positif tepat diimbangi oleh muatan negatif dari elektron
yang mengelilinginya. Nomor atom (atomic number) suatu unsur senyawa organik sama dengan jumlah
proton didalam inti (dan dengan jumlah elektron di sekitar inti dalam atom
netral). Bobot atom (atomic weight) kira-kira sama dengan jumlah proton dan
jumlah neutron di dalam inti, bobot elektron tidak diperhitungkan karena
ringannya.
Tabel1.1
jumlah orbital dan elektron dalam tiga kulit pertama
|
Nomor kulit
|
Jumlah orbital disetiap jenis
|
Jumlah elektron jika kulit penuh
|
||
|
s
|
p
|
d
|
||
|
1
|
1
|
0
|
0
|
2
|
|
2
|
1
|
3
|
0
|
8
|
|
3
|
1
|
3
|
5
|
18
|
Elektron
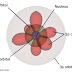
terpusat di kawasan tertentu di ruang sekitar inti yang dinamakan orbital.
Setiap orbital dapat menampung tidak lebih dari 2 elektron. Orbital, yang
bentuknya berbeda–beda, di tandai dengan huruf s, p, dan d. Selain itu,
orbital dikelompokkan dalam kulit (shell) yang diberi nomor 1,2,3 dst. Setiap
kulit mengandung jenis dan jumlah orbital yg berbeda-beda, bergantung pada
nomor kulitnya. Misalnya, kulit 1 hanya mengandung satu jenis orbital, disebut
dengan orbital 1s.
Tabel
1.2 susunan elektron dalam 18 unsur pertama
|
Nomor atom
|
Unsur
|
Jumlah elektron di setiap orbital
|
||||
|
1s
|
2s
|
2p
|
3s
|
3p
|
||
|
1
|
H
|
1
|
|
|
|
|
|
2
|
He
|
2
|
|
|
|
|
|
3
|
Li
|
2
|
1
|
|
|
|
|
4
|
Be
|
2
|
2
|
|
|
|
|
5
|
B
|
2
|
2
|
1
|
|
|
|
6
|
C
|
2
|
2
|
2
|
|
|
|
7
|
N
|
2
|
2
|
3
|
|
|
|
8
|
O
|
2
|
2
|
4
|
|
|
|
9
|
F
|
2
|
2
|
5
|
|
|
|
10
|
Ne
|
2
|
2
|
6
|
|
|
|
11
|
Na
|
2
|
2
|
6
|
1
|
|
|
12
|
Mg
|
2
|
2
|
6
|
2
|
|
|
13
|
Al
|
2
|
2
|
6
|
2
|
1
|
|
14
|
Si
|
2
|
2
|
6
|
2
|
2
|
|
15
|
P
|
2
|
2
|
6
|
2
|
3
|
|
16
|
S
|
2
|
2
|
6
|
2
|
4
|
|
17
|
Cl
|
2
|
2
|
6
|
2
|
5
|
|
18
|
Ar
|
2
|
2
|
6
|
2
|
6
|
Kulit
2 memuat dua jenis orbital, yaitu 2s
dan 2p, dan kulit 3 mengandung tiga
jenis, 3s, 3p, dan 3d. Dalam kulit
tertentu, jumlah orbital s, p, dan d ialah masing-masing 1, 3, 5 (tabel
1.1). Aturan ini memungkinkan kita menhitung berapa banyak elektron akan berada
di dalam kulit apabila kulit tersebut penuh (laju terakhir dalam Tabel 1.1).
Tabel 1.2 menunjukkan bagaimana susunan elektron 18 unsur pertama.
Kulit pertama diisi penuh oleh He
dan semua unsur sesudahnya, dan kulit kedua di isi penuh oleh Ne dan semua
unsur sesudahnya. Kulit yang terisi penuh hampir tidak berperan dalam ikatan
kimia. Sebaliknya, elektron terluar, atau elektron valensi, adalah yang
terutama terlibat dalam ikatan kimia.
Description: Bagaimana elektron tersusun dalam atom,
Rating: 4.5,
Reviewer: Unknown,
ItemReviewed: Bagaimana elektron tersusun dalam atom


JAMUEL SWEET & CASINO, LAKE EAST STREET, OK | JAMUEL SWEET & CASINO
ReplyDeleteJAMUEL SWEET & CASINO, LAKE 출장마사지 EAST 상주 출장마사지 STREET, OK. 0 reviews. $10. 1 bed. $10. $20. 서울특별 출장샵 1 bath. $10. $18. 1 bath. $10. $20. 1 bath. $10. $20. 충청북도 출장안마 1 bath. $10. $18. 순천 출장마사지 1 bath. $10.